铁对废水微生物脱氮的影响研究进展
【南通去离子水设备http://www.xqccs.cn】微生物脱氮是一种经济有效的治理水体氮污染的手段。目前微生物脱氮过程主要有厌氧氨氧化、硝化、反硝化及同时硝化反硝化等。铁是环境中普遍存在的金属元素,也是微生物所需的重要微量元素之一。在微生物脱氮系统中,铁盐或者含铁固体化合物等的投加会对微生物及脱氮工艺过程等产生一定的影响,且对于不同种类的微生物与不同的脱氮工艺,铁所产生的影响也将不同。本文全面综述了近些年的研究报道中铁对厌氧氨氧化、硝化、反硝化及同时硝化反硝化等不同脱氮过程中含氮污染物去除效果的影响,铁与脱氮微生物的酶活性、电子传递、增殖富集及脱氮反应器中生物膜、污泥絮体及颗粒形成等之间的作用关系,旨在全面理解铁对微生物脱氮系统的作用与内在机制,为实现利用铁强化微生物脱氮过程、提高微生物脱氮效率提供借鉴。
工业污水、农业污水及生活污水等往往存在着多种含氮污染物,包括氨氮、亚硝酸盐氮、硝酸盐氮等,对环境生态造成严重危害[1,2]。微生物脱氮具有处理彻底、无二次污染及经济等优点而被用于含氮废水的处理[3],其基本原理是利用微生物的同化或异化作用,将废水中的含氮化合物转化为生物质或氮气等气态产物而从废水中彻底去除。目前主要的微生物脱氮过程有厌氧氨氧化、硝化(氨氮、亚硝酸盐氮的好氧氧化)、反硝化(硝酸盐氮、亚硝酸盐氮被还原为气态产物氮气等)及同时硝化反硝化等。
铁是地球上含量较多的金属元素,来源广泛、价廉易得。同时,铁也是生物系统中最丰富的过渡金属元素,可与碳、氧、硫和氮等形成多种络合物[4],是微生物所需的重要微量元素之一[5]。微量元素铁能够促进微生物的电子传递、酶的合成等,纯水设备提高微生物活性和对氮的利用与转化[6]。含零价、二价及三价等不同价态和不同化学形态的铁单质或化合物,其对微生物脱氮过程造成的影响也会有所差别[7,8,9,10]。含氮废水脱氮过程涉及不同种类的微生物,对铁的需求或铁对其产生的影响也会不同,过量的铁可能抑制微生物的活性,造成微生物的中毒或死亡南通去离子水设备,因此需要研究实际情况中铁对微生物脱氮过程的影响,以确定含铁物质的适宜投加形式与用量[6,11]。
全面理解铁对微生物脱氮过程的影响及作用机制,对于利用铁提高微生物脱氮活性,改善微生物脱氮工艺,促进含氮废水的高效处理具有积极意义。本文全面综述了近些年来的研究报道中铁对厌氧氨氧化、硝化、反硝化及同时硝化反硝化等不同微生物脱氮过程中含氮污染物去除过程的影响,以及铁与脱氮微生物的酶活性、电子传递、增殖富集及脱氮反应器中生物膜、污泥絮体及污泥颗粒等之间的作用关系,旨在全面理解铁对微生物脱氮过程的影响及其产生的内在机制,为实现在实际生产中利用铁强化微生物脱氮过程提供借鉴。
1 铁对废水微生物脱氮的影响
目前用于废水脱氮的微生物过程主要有厌氧氨氧化、硝化、反硝化及同时硝化反硝化等。
1.1 厌氧氨氧化
厌氧氨氧化菌在厌氧条件下能够以氨氮为电子供体、亚硝酸盐氮为电子受体,将氨氮与亚硝酸盐氮同时转化为氮气,可用于处理高氨氮废水[12]。而为了提高厌氧氨氧化中的脱氮效率、缩短反应器启动时间,强化厌氧氨氧化脱氮效果,研究者对铁在不同投加形式和投加量下对厌氧氨氧化脱氮效果的影响开展了广泛的研究(表1)。
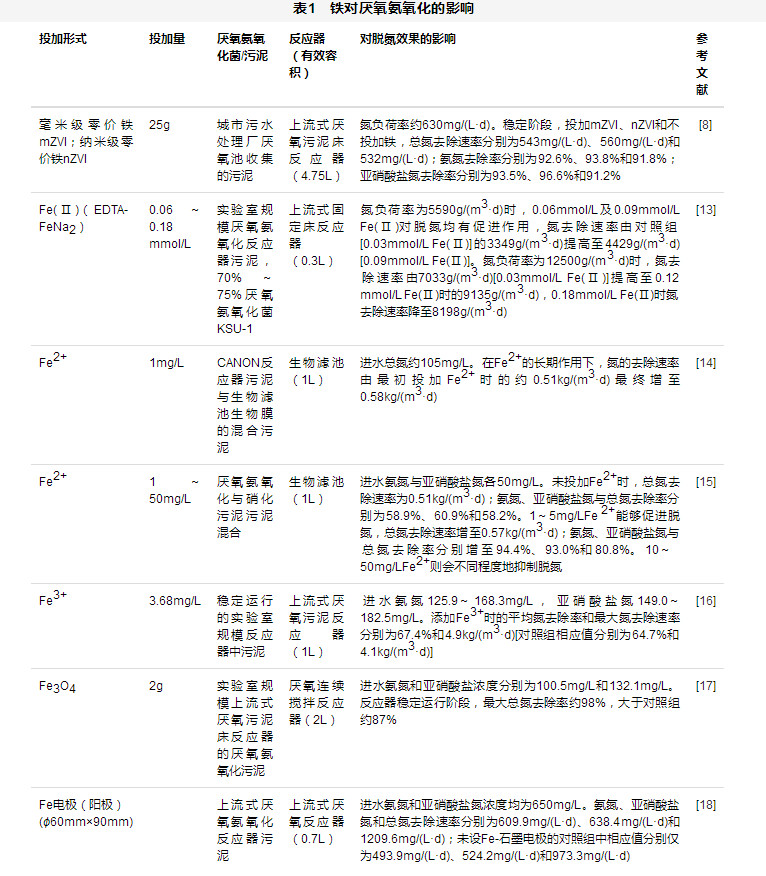
离子形式的铁(Fe2+或Fe3+)以及与EDTA-2Na螯合的二价铁Fe(Ⅱ)(EDTA-FeNa2)等被添加到厌氧氨氧化反应器中,用于促进微生物的厌氧氨氧化脱氮[13,14,15,16]。如表1所示,Fe2+或Fe3+在浓度为1~5mg/L以及Fe(Ⅱ)在浓度为0.06~0.12mmol/L(约3.35~6.72mg/L)时,均能提高厌氧氨氧化脱氮效果[13,14,15,16]。而当铁离子浓度过高时,反而会抑制厌氧氨氧化。在厌氧氨氧化生物滤池反应器中,当Fe2+添加浓度(10~20mg/L)超出适宜浓度范围1~5mg/L时,厌氧氨氧化受到抑制,过量的Fe2+将被吸附于厌氧氨氧化生物膜上,以缓解对脱氮的抑制作用,而当Fe2+浓度继续增加(30~50mg/L),超出了厌氧氨氧化生物膜对Fe2+的吸附容量时,不能被生物膜吸附的Fe2+将进入微生物细胞内,严重抑制微生物活性,降低脱氮效果,这种抑制将是不可逆转的[15]。
零价铁(ZVI)、四氧化三铁(Fe3O4)等固体形态的含铁物质,在水溶液中能够通过水解或解离释放出铁离子(Fe2+和Fe3+),也可用于促进厌氧氨氧化脱氮[8,17](表1)。Ren等[8]研究了不同尺度的ZVI材料,包括毫米级零价铁(mZVI)和纳米级零价铁(nZVI),结果表明,在上流式厌氧污泥床反应器中,mZVI和nZVI的投加均能提高厌氧氨氧化对含氮污染物的去除速率或去除率,且nZVI对厌氧氨氧化脱氮的促进效果优于mZVI。ZVI水解产生Fe2+促进厌氧氨氧化脱氮,同时也可作还原剂将硝酸盐通过化学作用还原为氨氮,去除硝酸盐的同时提供了充足的厌氧氨氧化底物[8]。nZVI相对于mZVI更能促进厌氧氨氧化脱氮的原因可能是nZVI具有比mZVI更高的活性[19]。投加到厌氧氨氧化系统中的ZVI快速水解产生的Fe3+在碱性条件下易转化为氢氧化铁[Fe(OH)3]红色絮状固体,沉积于厌氧氨氧化污泥颗粒的表面,抑制厌氧氨氧化菌活性,因此,随着反应器运行时间的延长,ZVI对厌氧氨氧化脱氮的作用将会由促进转为抑制[17]。Fe3O4也能够溶于水解离出Fe2+和Fe3+,与ZVI不同的是,Fe3O4的离子化速率与厌氧氨氧化系统对Fe2+和Fe3+的消耗速率保持平衡,在厌氧氨氧化系统中投加Fe3O4时未检测到Fe(OH)3生成,Fe2+和Fe3+浓度保持稳定,从而对厌氧氨氧化产生更稳定的促进作用[17]。
厌氧氨氧化反应器的启动耗时较长,适量铁的添加能够缩短厌氧氨氧化反应系统启动时间[13]。Ren等[8]的研究表明mZVI和nZVI的投加能使上流式厌氧污泥床反应器中厌氧氨氧化启动时间由126天分别缩短到105天和84天;Bi等[20]通过投加0.09mmol/L Fe2+使上流式厌氧氨氧化反应器的启动时间由70天缩减至50天。厌氧氨氧化反应器启动时间的缩短,促进了厌氧氨氧化技术在实际废水脱氮中的应用。
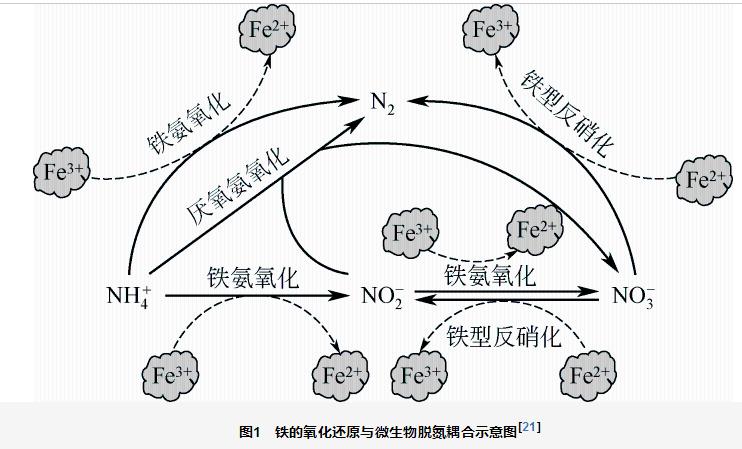
Li等[21]提出了一种将厌氧氨氧化与铁氨氧化、铁型反硝化耦合的新型脱氮过程,能够同时脱除一些废水中同时存在的氨氮和硝酸盐氮(图1):①通过铁氨氧化,微生物利用Fe3+为电子受体将氨氮氧化为亚硝酸盐氮、硝酸盐氮或氮气,同时Fe3+被还原为Fe2+;②通过铁型反硝化,微生物利用①中生成的Fe2+为电子供体还原硝酸盐氮为亚硝酸盐氮或氮气,而Fe2+又被氧化为Fe3+;③系统中剩余的氨氮与前述两个过程中的亚硝酸盐氮在厌氧氨氧化菌的作用下最终也转化为氮气,氮的转化过程与铁的转化过程(Fe2+和Fe3+)相结合,铁相当于该耦合脱氮过程的催化剂。在该耦合脱氮反应系统中,Fe3+添加浓度为30mg/L,经过62天的运行,氨氮和硝酸盐氮出水浓度由相同的进水浓度50mg/L分别降低至16.2mg/L和20.6mg/L,有效实现了氨氮与硝酸盐氮的同时去除[21]。
1.2 硝化
在硝化培养基中添加0.05~0.2mg/L Fe2+,即能促进哈尔滨不动杆菌对氨氮的异养硝化作用,其中,在Fe2+的最适添加浓度0.1mg/L下,哈尔滨不动杆菌对氨氮的硝化速率由未添加Fe2+时的0.19mg/(L·h)显著提高至0.50mg/(L·h)[22]。王秀蘅等[23]在对厌氧好氧脱氮工艺中好氧段氨氮硝化过程的研究中发现,5~20mg/L Fe2+的添加能够促进微生物对氨氮的硝化作用,南通去离子水设备其中20mg/L Fe2+的投加最高可使微生物对氨氮的转化率由0mg/L Fe2+时的约43%提高至约54%,而随着Fe2+投加量继续增加(20~80mg/L),这种促进作用有所减弱,但未达到产生毒性积累而抑制脱氮的程度。
在序批式生物膜反应器中装填含ZVI复合载体(生物海绵铁),反应器运行的稳定阶段和出水回流阶段氨氮去除率分别为60.6%和72.8%,而在装填不含ZVI载体的反应器中,相应阶段氨氮去除率分别仅为13.5%和16.8%,ZVI对氨氮硝化的促进作用显著[24]。Ma等[25]的研究表明,序批式活性污泥反应器在60mg/L磁性Fe3O4纳米粒子长期作用下,氨氮氧化速率受到磁性Fe3O4纳米粒子的抑制,由未添加磁性Fe3O4纳米粒子时的约5.2mg N/(gMLVSS·h)(MLVSS表示混合液挥发性悬浮固体浓度)降低至约4.7mg N/(g MLVSS·h),而亚硝酸盐氮硝化速率则由约4.9mg N/(g MLVSS·h)提高至7.10mg N/(g MLVSS·h)。从氨氮去除效果来看,随着磁性Fe3O4纳米粒子浓度由0增加到60mg/L,活性污泥反应器对氨氮的去除率基本稳定在98.50%左右,此浓度范围的磁性Fe3O4纳米粒子对硝化效果没有显著影响[25]。
1.3 反硝化
1.3.1 传统反硝化
Pintathong等[26]对泛营养副球菌P16反硝化过程的研究表明,硝酸盐氮初始浓度为700mg/L时,在培养基中添加1.5μmol/L Fe3+,48h后硝酸盐氮去除率由对照组(未添加Fe3+)的30.9%提高至51.8%。Fe3+长期作用于序批式活性污泥反应器时,低浓度的Fe3+(不超过40mg/L)能够促进反硝化脱氮,其中,Fe3+添加浓度为20mg/L和40mg/L时,总氮去除率相近,分别为89.7%和89.8%,高于对照组(0mg/L Fe3+)85.1%的总氮去除率;而当Fe3+投加浓度增至60mg/L时,则会抑制微生物脱氮,总氮去除率降至76.4%,低于对照组[27]。

在60mg/L磁性Fe3O4纳米粒子的长期作用下,序批式活性污泥反应器中硝酸盐氮还原速率由不添加磁性Fe3O4纳米粒子时的约12.10mg N/(g MLVSS·h)提高至18.64mg N/(g MLVSS·h),出水硝酸盐氮浓度比无磁性Fe3O4纳米粒子添加时降低了39.9%,而亚硝酸盐氮还原速率则由不添加磁性Fe3O4纳米粒子时的11.32mg N/(g MLVSS·h)降至10.41mg N/(g MLVSS·h),相应的出水亚硝酸盐氮浓度由几乎为0到最终稳定在0.06mg/L[25]。总的来看,60mg/L磁性Fe3O4纳米粒子的长期作用能够对序批式活性污泥反应器的反硝化过程产生促进作用[25]。
1.3.2 氢自养反硝化
氢自养反硝化菌以氢气为电子供体通过反硝化作用还原硝酸盐,该过程产生有机物量少、反硝化效率高,然而由于氢气成本高、易爆炸,其应用受限[28,29]。浸入水中的零价铁纳米颗粒通过电化学腐蚀作用产氢,能够为氢自养反硝化菌——真养产碱杆菌(Alcaligenes eutrophus)提供氢气作电子供体,从而实现对硝酸盐的还原和去除[29]。
1.3.3 铁型反硝化
利用铁化学还原法去除污染水体中的硝酸盐氮时,硝酸盐氮的还原产物为氨氮,不能彻底脱氮,且该反应需在较低的pH条件下进行[30]。而将硝酸盐反硝化与亚铁氧化过程耦合,通过微生物以亚铁为电子供体进行的反硝化作用,硝酸盐转化为氮气而被彻底脱除,即铁型反硝化[31,32]。不同形式含铁物质作电子供体的铁型反硝化过程在水体微生物脱氮中的应用见表2。
Lu等[33]将零价铁应用于微生物自养反硝化,菌株CC76兼具厌氧反硝化与还原铁功能,可利用零价铁在水溶液中氧化生成的Fe2+作电子供体,通过反硝化作用除去水体中的硝酸盐,Fe2+被氧化为Fe3+后又被CC76菌还原,实现了铁的循环。张宁博等[34]通过在反应器中投加还原铁粉实现了铁型反硝化,并通过改进反应器回流方式解决了副产物三价铁的氢氧化物等引起的污泥矿化与硝酸盐还原活性降低的问题。Zhou等[36]在上流式生物滤池中实现铁型反硝化脱氮,以Fe(Ⅱ) [Fe(Ⅱ)EDTA]为电子供体时,最大脱氮效率接近90%。在硝酸盐氮、亚硝酸盐氮与Fe2+共存的环境水体中,生物反硝化与铁氧化过程耦合可实现氮与铁同时去除(其中,Fe2+生成羟基氧化铁FeOOH沉淀)[35]。铁型反硝化脱氮污泥中高含量的铁化合物还可与磷酸盐类污染物结合形成磷酸铁等沉淀,实现含铁污泥的回收利用与同时脱氮除磷[37]。
固体形态的亚铁化合物,包括硫化亚铁(FeS)[38]、氢氧化亚铁[Fe(OH)2][38]、黄铁矿(FeS2)[39]、磁黄铁矿(Fe1-xS,x=0~0.125)[40]及菱铁矿(FeCO3)[41]等也能够为铁型反硝化过程提供电子供体。Wei等[38]利用污水处理厂富铁污泥中的氢氧化亚铁和硫化亚铁为硝酸盐自养反硝化提供电子供体,既实现了有效脱氮,又能使富铁污泥得到合理处置。Torrentó等[39]以黄铁矿FeS2为电子供体实现微生物对地下水中硝酸盐氮的反硝化还原。Li等[40]和Yang等[41]分别利用磁黄铁矿和菱铁矿作为微生物铁型反硝化的电子供体,实现废水同时脱氮除磷。固体亚铁化合物作电子供体时,硝酸盐氮还原速率与含铁物质的类型与表面积等因素密切相关[38,39]。
Zhang等[42]将铁碳微电解(IC-ME)与生物反硝化耦合用以处理低COD/硝酸盐比煤气化废水中的硝酸盐。其中,IC-ME载体由零价铁废料和碳为原料制得,在该耦合体系中,零价铁通过电化学腐蚀作用释放出Fe2+,为硝酸盐反硝化提供电子供体。该耦合过程与铁屑直接作电子供体相比,加快了铁的腐蚀与电子供体Fe2+的释放,总氮去除率也提高了16.64%[42]。
1.4 同时硝化反硝化
好氧反硝化菌的发现使得硝化作用和反硝化作用能够在同一反应器中同时进行,从而实现废水微生物脱氮,该过程即同时硝化反硝化[43]。Chen等[44]研究表明,在同时硝化反硝化活性污泥反应器中添加车床切割废料中的铁屑,废水的总氮浓度由25mg/L降至14mg/L,而在不加废铁屑的对照组中,虽然大部分氨氮能够通过硝化作用转化为硝酸盐氮,总氮含量却未见明显下降,废铁屑的添加主要是促进了好氧反硝化,进而使得同时硝化反硝化脱氮得以实现。投加废铁屑的实验组反应器中污泥中总Fe3+浓度为22.9mg/L,远高于对照组的3.2mg/L,而Fe2+浓度则低到可以忽略,因此对比可推测废铁屑释放出的Fe3+是同时硝化反硝化脱氮效率得以提高的重要原因;但若在反应器中直接投加等量的Fe3+,其对同时硝化反硝化脱氮效率的促进作用则不及投加废铁屑,因此废铁屑在同时硝化反硝化过程中的具体作用仍需进一步研究[44]。
2 铁对废水微生物脱氮的作用机制
2.1 酶的活性
铁是微生物生长必需的重要微量元素之一,在脱氮微生物酶的合成过程中起重要作用。在厌氧氨氧化过程中,铁能够促进厌氧氨氧化菌对铁的积累和血红素c的合成[13,18],血红素是厌氧氨氧化菌进行联氨脱氢酶(HDH)、联氨合成酶(HZS)、羟胺氧化还原酶(HAO)和亚硝酸盐还原酶(NIR)等酶组装的重要辅因子,参与厌氧氨氧化菌的代谢与增殖,促进厌氧氨氧化脱氮[20,45]。Qiao等[13]的研究表明,在厌氧氨氧化系统中,0.12mmol/L Fe(Ⅱ) [Fe(Ⅱ)EDTA]存在时,催化联氨转化为氮气的联氨脱氢酶HDH的活性比0.03mmol/L Fe(Ⅱ)或0.18 mmol/L Fe(Ⅱ)存在时分别提高了32.6%和73.2%,联氨脱氢酶HDH活性的变化与厌氧氨氧化脱氮速率变化趋势相一致。因此,适宜浓度Fe(Ⅱ)的添加是对厌氧氨氧化系统微量元素Fe的补充,能够提高联氨脱氢酶HDH的活性,促进厌氧氨氧化脱氮,而Fe(Ⅱ)添加 浓度过高时反而抑制联氨脱氢酶HDH的活性,抑制脱氮作用[13,20]。
硝化和反硝化过程中涉及多种生物催化酶,包括氨单加氧酶(AMO)、羟胺氧化还原酶(HAO)及亚硝酸氧化还原酶(NXR)等硝化酶[46,47],以及硝酸盐还原酶(NAR)、亚硝酸盐还原酶(NIR)、一氧化氮还原酶(NOR)和一氧化二氮还原酶(N2OR)等反硝化酶[11,44,48],铁是构成这些酶的重要金属元素之一[11,48]。Qian等[47]的研究表明在10~20℃温度范围内Fe2+的添加对氨单加氧酶AMO、羟胺氧化还原酶HAO和亚硝酸氧化还原酶NXR这3种酶的活性均有促进作用,其中氨单加氧酶AMO的活性增长最显著,比对照组提高了约14%~28%。Jia等[27]的研究则表明,适宜浓度(20~40mg/L)的Fe3+对硝酸盐还原酶NAR、亚硝酸盐还原酶NIR和一氧化氮还原酶NOR活性有一定的促进作用,其中Fe3+对一氧化氮还原酶NOR活性的促进作用最为显著,比对照组一氧化氮还原酶NOR活性高约10%~16%,而60mg/L的过量Fe3+投加则会形成三价铁的氧化物或氢氧化物包覆在反硝化微生物细胞表面,破坏细胞结构,抑制反硝化酶的活性,进而抑制反硝化脱氮[27]。在同时硝化反硝化系统中添加废铁屑时,编码硝酸盐还原酶的基因NapA和亚硝酸盐还原酶的基因NirK、NirS的表达量分别是未添加铁屑时的2.24倍、6.87倍和5.45倍,氨单加氧酶AMO、亚硝酸盐氧化还原酶NXR、硝酸盐还原酶NAR和亚硝酸盐还原酶NIR的活性分别提高到无废铁屑添加时的1.23倍、1.53倍、3.60倍和1.55倍,相应总氮去除率也比对照组显著提高[44]。
磁性纳米粒子投加到硝化反硝化脱氮系统的初期,因其对微生物的急性生物毒性而抑制微生物脱氮;而由于活性污泥的自修复作用及磁性材料的磁效应对微生物的促进作用等,磁性纳米粒子长期作用时将对微生物脱氮酶的活性及脱氮效果产生一定的促进作用[9]。在60mg/L磁性Fe3O4纳米粒子长期作用下,序批式活性污泥反应器中氨单加氧酶AMO、亚硝酸盐还原酶NIR活性仍然受到一定程度的抑制,分别比未添加磁性Fe3O4纳米粒子时降低了26%和13%,而亚硝酸盐氧化还原酶NXR和硝酸盐还原酶NAR活性则分别比未添加磁性Fe3O4纳米粒子时提高了16%和26%,南通去离子水设备而相应的氨氮去除效果几乎不受影响,硝酸盐氮去除率有所提高[25]。另有研究表明50mg/L磁性纳米粒子长期作用于序批式活性污泥反应器时,亚硝酸盐氧化还原酶NXR、硝酸盐还原酶NAR和亚硝酸盐还原酶NIR活性分别比未投加磁性纳米粒子时提高了12%、23%和27%,而氨单加氧酶AMO的相对活性则与对照组相似[9]。磁性纳米粒子的长期作用表现出对不同硝化或反硝化酶的或促进或抑制作用,其中具体的作用机制有待研究者进一步研究。
2.2 电子传递
铁是脱氮微生物细胞的电子传递载体细胞色素c、细胞色素bc1复合体等的活性中心[13,23,44,47],通过还原态Fe2+与氧化态Fe3+之间的氧化还原循环过程实现单电子的传递[49],在脱氮微生物电子传递系统中具有重要作用。铁也能够直接参与微生物脱氮过程中的电子传递,促进氮的转化或去除。研究者在对厌氧氨氧化的研究中发现,微生物能够利用Fe2+作还原剂或电子供体,将硝酸盐氮还原为亚硝酸盐氮[17,45,50],或利用Fe3+作电子受体,将部分氨氮转化为亚硝酸盐氮或硝酸盐氮[17,51],从而影响厌氧氨氧化的底物浓度。而在厌氧氨氧化与铁氨氧化、铁型反硝化耦合同时去除氨氮和硝酸盐氮的过程中,相互转化的Fe2+和Fe3+分别起电子供体和电子受体的作用,该过程涉及的氮转化与铁循环的化学式见表3[21]。还原性铁ZVI可作还原剂,将硝酸盐还原为氨氮,为厌氧氨氧化提供适宜的底物浓度,同时去除了硝酸盐氮[8]。相对于传统的反硝化过程,氢自养反硝化和铁自氧反硝化分别由铁参与反应产生的氢作为电子供体或铁直接作为电子供体,在铁自身被氧化的同时,实现硝酸盐的还原与去除[29,32]。铁作为电子供体或受体,与各微生物脱氮过程之间的作用所涉及的化学式见表3。

2.3 微生物及微生物群落
铁是厌氧氨氧化菌生长的重要微量元素,能够提高厌氧氨氧化菌活性、促进厌氧氨氧化菌增殖[17,45],还原性铁ZVI可作脱氧剂,消耗掉厌氧氨氧化系统中的溶氧,为厌氧氨氧化菌的增殖提供厌氧环境[8],铁离子(Fe2+、Fe3+)带正电荷,因此能够吸附细胞表面带负电荷的厌氧氨氧化菌,形成厌氧氨氧化颗粒,促进微生物在反应器中的富集[17]。在添加mZVI或nZVI的厌氧氨氧化反应器中,厌氧氨氧化菌细胞的丰度是不添加ZVI的对照组的近10倍[8]。在厌氧氨氧化生物滤池中,Fe2+的添加使厌氧氨氧化菌(Candidatus Kuenenia)的相对丰度由7.99%提高到11.30%[14]。在厌氧氨氧化与铁氨氧化、铁型反硝化耦合的脱氮过程中,Fe3+及Fe2+能够使具有氨氮氧化作用的铁还原菌假单胞菌(Pseudomonas)、地杆菌(Geobacter)和具有硝酸盐还原作用的亚铁氧化菌硫杆菌(Thiobacillus)得以富集,在微生物群落中的相对丰度高于仅有厌氧氨氧化作用的对照组,这些微生物相对丰度的增加与脱氮系统对氨氮及硝酸盐氮去除率的增加相一致[21]。
铁也能够促进硝化或反硝化菌的增殖,显著影响微生物群落结构。在序批式生物膜反应器中ZVI的加入使异养硝化菌产碱杆菌(Alcaligenes)在反应器细菌总数中的比例由36.5%显著提高到67.5%[24]。在序批式活性污泥反应器中Fe2+的添加能够提高亚硝化单胞菌(Nitrosomonas)及硝化杆菌(Nitrobacter)等自养硝化菌的相对丰度与生物量[9,47]。在序批式活性污泥反应器中,随着磁性Fe3O4纳米粒子投加浓度由0逐渐增加到60mg/L,微生物的丰度与多样性也发生变化,其中陶厄氏菌(Thauera)、丛毛单胞菌(comamonas)及生丝微菌(Hyphomicrobium)等反硝化菌在活性污泥微生物群落中的相对丰度呈增长趋势,这与Fe3O4纳米粒子在60mg/L时对反硝化的促进作用相一致[25]。铁型反硝化过程中Fe2+能够富集铁型反硝化菌嗜酸菌(Acidovorax)和硫杆菌(Thiobacillus)等,从而促进脱氮[42]。废铁屑的添加使得同时硝化反硝化脱氮系统中好氧反硝化菌包括陶厄氏菌(Thauera)、嗜热单胞菌(Thermomonas)、红杆菌(Rhodobacter)和生丝微菌(Hyphomicrobium)等的总相对丰度由不含废铁屑对照组中的1.452%增长到3.575%,好氧反硝化菌得以在反应器中富集并发挥反硝化作用,进而促进同时硝化反硝化过程的实现,提高微生物的脱氮效果[44]。
2.4 生物膜、污泥絮体及颗粒的形成
在厌氧氨氧化生物滤池中,Fe2+对厌氧氨氧化菌的活性与增殖等的促进作用使得反应器中形成的生物膜转变为红色且更加紧实[14]。铁离子还能够通过混凝和絮凝作用改善污泥的沉降性能,促进微生物脱氮[27]。Fe2+和Fe3+都是有效的活性污泥絮凝剂,与Fe3+相比,投加Fe2+的污泥中絮体菌丝更紧密,沉降性能更好[53]。铁对于脱氮系统污泥颗粒的形成具有重要作用,研究表明在活性污泥脱氮反应器中,不同形态铁的投加能够促进污泥颗粒的形成,增强污泥颗粒的稳定性,主要表现在:①Fe3O4等可作污泥颗粒化的核心[17,54],铁离子带正电荷,中和微生物表面负电荷,促进微生物的聚集[18,54],同时作为桥联离子,与胞外多糖聚合物形成网络,促进污泥的颗粒化[55];②促进微生物分泌胞外聚合物(EPS),提高污泥造粒相关微生物的活性和丰度,加速污泥颗粒化,提高污泥颗粒稳定性[9,42,54];③抑制丝状突起的生长,防止丝状细菌的过度生长导致的颗粒解体,改善污泥颗粒形态,有利于形成光滑致密的污泥颗粒[17,54];④在投加铁的厌氧氨氧化反应器的污泥颗粒内部,一部分铁离子被用于合成微生物细胞结构,从而在污泥颗粒内部形成孔洞,这将有利于微生物脱氮产生的氮气及时从污泥颗粒内部排出,避免了污泥颗粒内部气压达到临界点而引起污泥颗粒的崩塌与解体[17]。
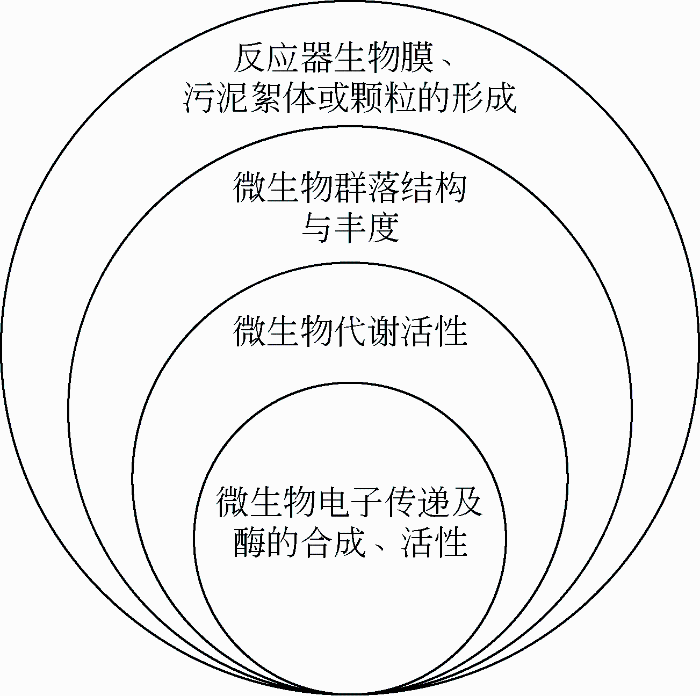
综上所述,研究者针对铁对废水微生物脱氮的作用机制进行了大量的探索,涵盖了微生物脱氮的多个方面(图2),从微生物电子传递、脱氮相关的酶等合成与活性,到微生物的生长增殖、对氮的转化及胞外聚合物EPS的分泌等代谢活性,再到微生物群落中物种结构与丰度的变化,最后到微生物反应器中的生物膜、絮体或污泥颗粒等的形成及特性。正是铁对微生物脱氮过程这些方方面面的作用共同实现了对微生物脱氮效果的促进作用。然而,上述关于铁对微生物脱氮作用机制的研究仍然是不够全面的。从微生物个体层面来看,关于铁的添加对于酶活性的具体作用机制的研究还不够深入[13],铁的添加对不同酶活性的促进作用或显著或不显著,甚至会产生抑制作用[25,27,47],这种差异化的影响产生的内在因素是什么,尚未得到明确分析,铁对编码相应酶的基因表达的作用与对酶活性的促进作用是否存在确切关联,仍需进一步研究。从微生物脱氮系统层面上看,整个系统包含着复杂的作用关系,有微生物与微生物、微生物与氮代谢、微生物与其他污染物的代谢等[17,56],铁的加入对微生物脱氮系统中存在的多种不同作用可能会产生复杂的影响,目前尚缺乏相关的系统化研究。此外,铁对微生物脱氮过程的多方面作用中的关键作用是什么,各方面的促进作用贡献程度是多大,如何实现铁对微生物脱氮系统的正向促进作用的最大化,这仍然依赖于进一步的机理方面的研究。未来可借助分子生物学手段,开展基因组、转录组、蛋白组等研究,揭示铁在脱氮微生物复杂生命活动中的具体作用,利用同位素示踪结合宏基因组、宏转录组等研究方法,揭示铁对微生物脱氮系统的促进作用机制,建立由点到面的网络化机理模型,为利用铁促进微生物脱氮提供更有力的理论支撑和指导。
铁对水体微生物脱氮有重要影响。投加适量的、不同化学形态的铁能够对多种微生物脱氮过程产生一定的促进作用,进而提高微生物对废水中含氮污染物的去除效果。铁对微生物脱氮的促进作用产生的内在机制是多方面的。铁是微生物生长必需的重要微量元素之一,能提高脱氮酶的活性,提高微生物活性,强化微生物脱氮效果。铁还可用作自养反硝化菌的电子供体,在自身被氧化的同时实现硝酸盐氮、亚硝酸盐氮的反硝化还原和去除。在厌氧氨氧化过程中微生物能够利用不同价态的铁离子作为电子受体将氨氮氧化为亚硝酸盐,或作电子供体将硝酸盐反硝化为亚硝酸盐,从而保证充足的厌氧氨氧化底物。微生物作用下的铁循环与氮循环过程的耦合能够同时实现氮的转化与去除和铁的循环与再利用。投加到微生物脱氮反应体系内的铁的转化产物还可与废水中其他污染物作用,如能够与磷酸盐等形成沉淀,实现同时脱氮除磷。铁还能够影响脱氮系统的微生物群落,促进脱氮微生物的富集,强化微生物脱氮效果。铁的添加改善了反应器性能,促进污泥颗粒的形成,提高了污泥颗粒稳定性及污泥絮体或污泥颗粒的沉降性能。全面理解铁对水体微生物脱氮的促进作用及其内在作用机制,有助于通过投加铁的方式有效强化水体微生物脱氮过程和含氮废水的治理,促进微生物脱氮过程的实际应用。
然而目前文献中关于铁对微生物脱氮的影响方面的报道多集中于现象与应用效果研究,而关于铁对微生物脱氮的内在作用机制的研究还不够系统和深入。同时,对不同种类的微生物、不同类型的反应器,铁对水体微生物脱氮过程起促进作用的阈值也各异,过量的铁反而会对微生物脱氮过程产生抑制作用;不同形式或价态的铁,如铁屑、铁粉、零价铁及二价或三价的铁离子,所产生的作用也有所差别,这其中的内在原因仍需进一步探究。结合目前已有研究,本文提出了以下几点未来的研究方向:①系统地研究不同赋存形态和不同浓度的铁的添加对微生物脱氮过程的影响、铁产生促进作用的适宜浓度范围及铁对微生物脱氮过程作用的时间效应,为铁在废水微生物脱氮过程中的应用提供有价值的参考;②研究铁与微生物脱氮系统中的其他环境因素(金属离子、有机/无机污染物等)可能存在的相互作用及对微生物脱氮系统的共同作用,更全面地了解铁对废水微生物脱氮的作用方式;③借助同位素示踪结合基因组、转录组、蛋白组等分子生物学研究方法研究铁的添加对微生物脱氮系统的影响,全面深入地揭示铁对微生物脱氮的促进作用机理,为应用铁促进废水微生物脱氮提供理论支撑和指导。南通水处理设备,南通去离子水设备。医院用水处理设备,医用GMP纯化水设备。
- 上一篇:污泥深度脱水板框压滤设备的质量控制和检测方法应用研究 2020/3/26
- 下一篇:南通纯水设备浅析城镇污水处理项目中结合运用PPP与专项债 2020/3/20
